Chirurgische Onkologie
Die NCT Standorte in Dresden und Heidelberg arbeiten an der Individualisierung chirurgischer Behandlungen in Form von Präzisionschirurgie. Eine gemeinsame Hauptmission ist die Etablierung des Forschungsfeldes der chirurgischen Datenwissenschaft, mit dem Ziel sowohl die Qualität, als auch den Wert der interventionellen Gesundheitsversorgung, zu verbessern. Dies geschieht durch die Aufnahme, Organisation, Analyse und Modellierung aller verfügbaren Daten der gesamten Behandlungskette. Die Entwicklung der zukünftigen Infrastruktur, der Werkzeuge und der Konzepte, die datengetriebene Onkologie und interdisziplinare Datenwissenschaft ermöglichen sollen, ist daher eine strategische Priorität. Beide NCT Standorte tragen eine führende Rolle in der Surgical Data Science Initiative (www.surgical-data-science.org), welche ins Leben gerufen wurde um die Sichtbarkeit der NCT Standorte als führende Institutionen im Bereich der chirurgischen Datenwissenschaft weiter zu erhöhen.
Forschungsprofil Dresden
Ein Fokus ist die Entwicklung und Evaluation computer- und robotergestützter Systeme, welche die kontextabhängige Verwendbarkeit verfügbarer Daten aus der gesamten chirurgischen Behandlungskette nutzen. Dies beinhaltet die Analyse chirurgischer Arbeitsabläufe, Navigation im Weichgewebe, intraoperative Visualisierung, chirurgisches Training und chirurgische Datenwissenschaft. In der viszeralen, urologischen und gynäkologischen Chirurgie werden robotergestützte Systeme klinisch evaluiert und weiterentwickelt. Im Feld der onkologischen Neurochirurgie liegt der Fokus der Forschung auf der bildgestützten Resektion, welche funktionale und hyperspektrale Bildgebung verwendet. Forschungsmöglichkeiten werden maßgeblich durch den NCT präklinischen Experimental Operationsraum (OR) unterstützt.
KI-gestützte Operation am Weichgewebe
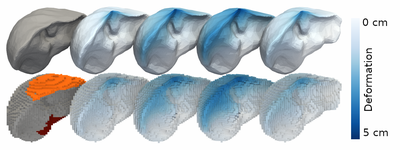
Ein Forschungsschwerpunkt ist die Echtzeit Analyse intraoperativer Sensoren zur kontextsensitiven Assistenz. Um die Navigation im Weichgewebe zu ermöglichen, bei der die Position des Tumors innerhalb eines Organs prognostiziert wird, wurde eine neuartige Methode präsentiert, welche die Deformation von Weichgewebe mittels Deep Learning und Simulationen erlernt. Das Ergebnis ist ein datengetriebenes Deformationsmodell, welches Echtzeit-Simulationen ermöglicht- hierbei erreicht es eine vergleichbare Genauigkeit wie modernste Systeme, während es aber um ein Vielfaches schneller arbeitet. Diese Methode wird momentan in interdisziplinären Kooperationsprojekten angewendet, mit dem Ziel, nutzerzentrierte, intraoperative Echtzeit-Navigationssysteme zu entwickeln, etwa für komplexe onkologische Leberoperationen.
Pfeiffer et al., Int J CARS 2019; Bodenstedt et al., Int J CARS 2019