veröffentlich am: 29.04.2026
MDS-Therapie: Dresdner Team zeigt Potenzial von Tasquinimod für verbesserte Blutbildung und Behandlung von Knochenschäden
Forscherinnen der Hochschulmedizin Dresden haben möglicherweise einen neuen Therapieansatz zur Behandlung myelodysplastischer Neoplasien (MDS) gefunden. In einer aktuellen Studie konnte das Team um Prof. Manja Wobus und Dr. Katja Sockel nachweisen, dass der entzündungshemmende Wirkstoff Tasquinimod in präklinischen Modellen sowohl die bei MDS gestörte Blutbildung verbessert als auch Knochenschäden reduziert. Damit adressieren sie zwei zentrale und eng miteinander verbundene klinische Probleme bei einer MDS-Erkrankung. Die entsprechende Studie zur präklinischen Wirksamkeit von Tasquinimod bei myelodysplastischen Neoplasien ist kürzlich in der Zeitschrift „HemaSphere“, einem Fachjournal für Hämatologie erschienen.
MDS oder myelodysplastische Neoplasien sind eine Vorstufe von Leukämie und gehören zu den Erkrankungen des Knochenmarks, bei denen die Bildung gesunder Blutzellen gestört ist. Dies führt häufig zu einer Anämie. Gleichzeitig haben viele Patientinnen und Patienten ein erhöhtes Risiko für Osteoporose, was auf Veränderungen im Knochenmark und entzündliche Prozesse zurückgeführt wird.

Mit diesem, in der präklinischen Studie erbrachten Proof of Concept kann die Forschung der Wissenschaftlerinnen in die nächste Phase gehen. Ziel ist es, entzündliche Signalwege im Knochenmark gezielt therapeutisch zu nutzen und den Wirkstoff in die klinische Entwicklung zu überführen. „Das wäre aus meiner Sicht der nächste und folgerichtige Schritt hin zu einer integrativen Behandlungsstrategie, die sowohl Blutbildung als auch Knochengesundheit berücksichtigt und damit langfristig die Versorgung vor allem von Patientinnen und Patienten mit Niedrigrisiko-MDS verbessern kann“, sagt Dr. Katja Sockel, Fachärztin für Innere Medizin, Hämatologie und Onkologie an der MKI sowie über das BMFTR geförderte Clinician Scientist in der translationalen Onkologie.
Die Ergebnisse unterstreichen einmal mehr die Bedeutung translationaler Forschung für Fortschritte in der Behandlung schwerer Erkrankungen. „Nur ein gezieltes Verständnis entzündlicher Prozesse im Knochenmark ermöglicht es, neue therapeutische Strategien zu entwickeln und in die klinische Praxis zu überführen“, erklären die Forscherinnen.
„Die gemeinsame Forschung durch eine Biologin und eine Ärztin in einem ‚Tandem‘ ist ein Modell, das sich in Dresden in der Bearbeitung komplexer Krebsforschungsprojekte sehr bewährt hat“, bestätigt Martin Bornhäuser, Direktor der MKI und einer der geschäftsführenden Direktoren des NCT/UCC Dresden. „Das NCT/UCC bietet ideale Voraussetzungen, um mit modernsten Methoden neue Ansätze in der Behandlung von Krebserkrankungen aus dem Labor kommend bis zur Anwendung am Patienten zu entwickeln.“
Die Studie:
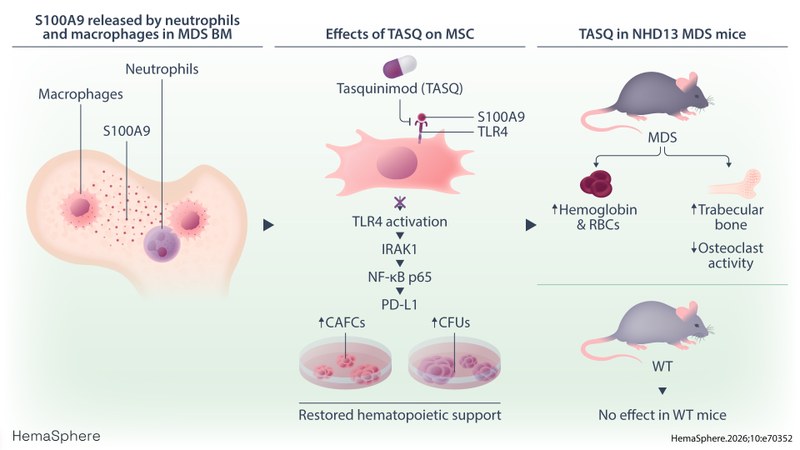
Tasquinimod (TASQ) hemmt den Entzündungsfaktor S100A9 und konnte in präklinischen MDS-Modellen die gestörte Blutbildung verbessern sowie Knochenverlust mindern. Die Autor:innen zeigen, dass im Knochenmark von MDS Patient:innen vor allem Neutrophile und Makrophagen S100A9 bereitstellen und dass TASQ die dadurch ausgelösten entzündlichen Signalwege in mesenchymalen Stromazellen unterdrückt. Entwickelt und zur Verfügung gestellt wurde Tasquinimod von Active Biotech (Lund, Schweden).
Zentrale Ergebnisse
- TASQ blockierte in vitro die S100A9-vermittelte Aktivierung von TLR4-Signalwegen und senkte Entzündungsmarker wie IL-1β, IL-18, Caspase-1 und PD-L1.
- Dadurch verbesserte sich die unterstützende Funktion der mesenchymalen Stromazellen für die Blutbildung; es entstanden mehr Kolonieformationen blutbildender Vorläuferzellen
- In MDS-Mäusen erhöhte die Behandlung mit TASQ Hämoglobin und Zahl der roten Blutkörperchen, hatte aber keinen negativen Effekt in gesunden Wildtyp-Mäusen.
- Außerdem verbesserte TASQ die Knochenstruktur, unter anderem durch mehr Trabekel und größeres Knochenvolumen, vermutlich weil die Osteoklastenaktivität sank.
Publikation:
Manja Wobus et. al, “Preclinical efficacy of tasquinimod in myelodysplastic neoplasms: Restoring erythropoiesis and mitigating bone loss”: http://dx.doi.org/10.1002/hem3.70352.
Kontakt:
Prof. Manja Wobus
Medizinische Klinik 1, Stammzelllabor 2
Universitätsklinikum Carl Gustav Carus an der Technischen Universität Dresden
Tel. +49 (0)351 458-14765
manja.wobus@ukdd.de
Anne-Stephanie Vetter
Stabsstelle Öffentlichkeitsarbeit Medizinische Fakultät Carl Gustav Carus
der Technischen Universität Dresden
Nationales Centrum für Tumorerkrankungen (NCT/UCC) Dresden
Tel.: +49 (0) 351 458 17903
anne-stephanie.vetter@tu-dresden.de



