Ein Konsortium der Onkologischen Spitzenzentren (Comprehensive Cancer Center) in Dresden, Frankfurt-Marburg und Leipzig/Jena entwickelt eine neuartige Gentherapie zur Behandlung eines besonders bösartigen hirneigenen Tumors (Glioblastom). Ziel ist es, gleichzeitig ein Tumor-unterdrückendes Gen (p53) in die Krebszellen einzuschleusen und Mechanismen zu unterbinden, welche die Genfunktion blockieren können. Hierfür entwickeln die Wissenschaftlerinnen und Wissenschaftler unter anderem ein neues Nanopartikel-Transportsystem. Das von Forschenden der Hochschulmedizin Dresden und am Nationalen Centrum für Tumorerkrankungen Dresden (NCT/UCC) geleitete Projekt „NANO-REPLACE“ wird von der Deutschen Krebshilfe mit rund einer Million Euro gefördert.
Das Nationale Centrum für Tumorerkrankungen Dresden (NCT/UCC) ist eine gemeinsame Einrichtung des Deutschen Krebsforschungszentrums (DKFZ), des Universitätsklinikums Carl Gustav Carus Dresden, der Medizinischen Fakultät Carl Gustav Carus der TU Dresden und des Helmholtz-Zentrums Dresden-Rossendorf (HZDR).
Das Glioblastom ist der häufigste und bösartigste hirneigene Tumor bei Erwachsenen. Betroffene haben auch mit modernster Therapie – in der Regel eine neurochirurgische Entfernung des Tumors, gefolgt von Chemotherapie und Strahlentherapie – nur eine mittlere Überlebenszeit von weniger als zwei Jahren. Weitere Verbesserungen in der Behandlung werden dringend benötigt.
Charakteristisch für Glioblastome ist ein Verlust der Funktion des tumorunterdrückenden Proteins p53, häufig verbunden mit Mutationen im p53-Gen, das den Bauplan für das Protein enthält. p53 kann so die unkontrollierte Teilung geschädigter Zellen nicht mehr unterdrücken. Die gentherapeutische Einschleusung des nicht-mutierten p53-Gens (Wildtyp) gilt als vielversprechende Therapieoption. Allerdings ist seit längerem bekannt, dass die in den Krebszellen vorhandene mutierte Genvariante das intakte Gen über verschiedene Mechanismen blockieren kann. „Wir verfolgen daher in einem neuartigen gentherapeutischen Ansatz das Ziel, gleichzeitig das Wildtyp-Gen einzuschleusen und das mutierte Gen und weitere molekulare Ziele zu blockieren. Dies soll letztendlich zum Absterben der Glioblastomzellen führen und das Fortschreiten der Tumorerkrankung hemmen“, sagt Prof. Achim Temme, Leiter der Neurochirurgischen Forschung der Hochschulmedizin Dresden.
„Die therapeutischen Möglichkeiten für Glioblastom-Patientinnen und -Patienten zu verbessern, ist uns ein wichtiges Anliegen. Wir freuen uns, dass drei der von uns geförderten Comprehensive Cancer Center ihre Kompetenzen zur Entwicklung einer vielversprechenden Gentherapie bündeln“, sagt Gerd Nettekoven, Vorstandsvorsitzender der Deutschen Krebshilfe. „Dieses wichtige Forschungsprojekt unterstützen wir im Rahmen eines gezielten Programmes, das das Ziel hat, Innovationen für die Krebsmedizin zu entwickeln und die klinische und translationale Krebsforschung voranzubringen. Neue Erkenntnisse aus der Grundlagenforschung sollen durch unsere Förderinitiative so schnell wie möglich den Patienten zugutekommen.“
Zur Blockade des in den Tumorzellen vorhandenen mutierten Gens nutzen die Forschenden einen speziellen Mechanismus zur Gen-Stilllegung, die so genannte RNA-Interferenz (RNAi). Hierbei wird durch eine Bindung von kurzen Ribonukleinsäure (RNA)-Stücken, sogenannte siRNAs, an die Erbgut-übertragende messenger-RNA (mRNA) deren Ablesung in ein Protein verhindert. Für die simultane Einschleusung eines für die Herstellung des funktionsfähigen Proteins optimierten (Codon-optimierten) Wildtyp-p53-Gens und der für die RNA-Interferenz nötigen RNA-Oligonukleotide (siRNAs) entwickeln die Forschenden ein neues, nicht-virales Nanopartikel-Transportsystem. „Oftmals werden Viren als Genfähren eingesetzt, die jedoch neue Mutationen und andere Nebenwirkungen auslösen können und technische Limitationen haben. Wir setzen hingegen auf nicht-virale, biologisch gut verträgliche Trägermoleküle. Diese bilden Nanopartikel, mit denen sich Gen und RNA gleichzeitig in die Tumorzelle einschleusen lassen und die darüber hinaus Gewebe durchdringen können“, betont Prof. Achim Aigner, Leiter der Selbständigen Abteilung für Klinische Pharmakologie im Rudolf-Boehm-Institut für Pharmakologie und Toxikologie der Universität Leipzig. „Künftig könnte bei der Operation des Glioblastoms ein Zugang gelegt werden, durch den dann die Gentherapie direkt am Ort des Tumorwachstums appliziert wird“, erklärt Prof. Achim Temme.
Neben der Entwicklung des Transport-Systems liegt ein wichtiger Fokus des Forschungsprojekts „NANO-REPLACE“ darin, die Effekte der neuartigen Gentherapie umfassend im Labor zu analysieren. Die Wissenschaftlerinnen und Wissenschaftler arbeiten hierzu mit Kulturen und Mini-Tumoren aus patienteneigenen Tumorzellen ebenso wie mit tumortragenden Mäusen. „Die Anwendung dieser Trägermoleküle testen wir in Kombination mit einer Blockade weiterer Zielproteine des Glioblastoms, welche die Selbstverdauung zellulärer Bestandteile, die sogenannte Autophagie, regeln. Diese Blockade soll verhindern, dass Tumorzellen dem p53-induzierten Zelltod auf anderem Wege entkommen", erklärt Prof. Donat Kögel, Gruppenleiter Experimentelle Neurochirurgie in der Klinik für Neurochirurgie des Universitätsklinikum Frankfurt.
Außer dem NANO-REPLACE-Projekt war in der 9. Ausschreibung des Förderschwerpunkts „Translationale Onkologie“ der Deutschen Krebshilfe noch ein weiteres standortübergreifendes Projekt unter Dresdner Federführung erfolgreich, das den Einsatz künstlicher Intelligenz für Diagnose, Prognose und Therapievorhersage bei Darmkrebs untersucht. „Wir freuen uns, dass unter Dresdner Leitung und durch die Förderung der Deutschen Krebshilfe wichtige Impulse ausgehen, um die Therapie und Diagnostik für Krebspatientinnen und -patienten weiter zu verbessern“, sagt Prof. Michael Albrecht, Medizinischer Vorstand des Universitätsklinikums Dresden.
Fakten zum Projekt:
• Projektlaufzeit: 1. April 2023 bis 31. März 2026 (drei Jahre)
• Konsortialpartner sind das Nationale Centrum für Tumorerkrankungen Dresden (NCT/UCC), das Universitäre Centrum für Tumorerkrankungen (UCT) Frankfurt-Marburg und das Mitteldeutsche Krebszentrum (CCCG) Leipzig/Jena.
• Das Projekt NANO-REPLACE („Genetische p53mut – Wildtyp-Substitution: Entwicklung einer dualen Nanopartikel-basierten Oligonukleotid-Therapie des Glioblastoms“) wird mit 955.015 Euro durch die Deutsche Krebshilfe gefördert.
Zur Pressemitteilung steht ein Bild in druckfähiger Auflösung zur Verfügung:
https://www.nct-dresden.de/fileadmin/media/nct-dresden/das-nct/newsroom/pressemitteilungen/Glioblastomzellen.jpg
Bildunterschrift:
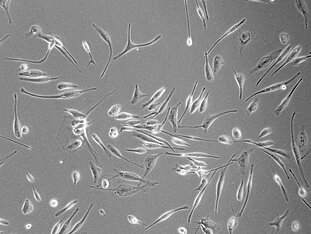
Frisch isolierte Glioblastomzellen eines Patienten in der Zellkultur (400-fache Vergrößerung). © Prof. Temme, Uniklinikum Dresden.
Nutzungshinweis für Bildmaterial zu Pressemitteilungen
Die Nutzung ist kostenlos. Das NCT/UCC Dresden gestattet die einmalige Verwendung in Zusammenhang mit der Berichterstattung über das Thema der Pressemitteilung. Bitte geben Sie als Bildnachweis an: „© Prof. Temme, Uniklinikum Dresden“. Eine Weitergabe des Bildmaterials an Dritte ist nur nach vorheriger Rücksprache mit der NCT/UCC-Pressestelle (Tel. 0351 458 5548, E-Mail: anna.kraft@nct-dresden.de) gestattet. Eine Nutzung zu kommerziellen Zwecken ist untersagt.
Ansprechpartner für die Presse:
Dr. Anna Kraft
Nationales Centrum für Tumorerkrankungen Dresden (NCT/UCC)
Presse- und Öffentlichkeitsarbeit
Tel.: +49 (0)351 458-5548
E-Mail: anna.kraft@nct-dresden.de
www.nct-dresden.de
Dr. Sibylle Kohlstädt
Deutsches Krebsforschungszentrum (DKFZ)
Strategische Kommunikation und Öffentlichkeitsarbeit
Tel.: +49 (0)6221 42-2854
Fax: +49 (0)6221 42-2968
E-Mail: s.kohlstaedt@dkfz.de
www.dkfz.de
Stephan Wiegand
Stabsstelle Öffentlichkeitsarbeit & Marketing
Medizinische Fakultät Carl Gustav Carus der Technischen Universität Dresden
Tel.: +49 (0) 351 458-19389
Fax: +49 (0) 351 458-885486
E-Mail: stephan.wiegand@tu-dresden.de
www.tu-dresden.de/med
Holger Ostermeyer
Universitätsklinikum Carl Gustav Carus Dresden Pressestelle
Tel.: +49 (0)351 458-4162
Fax: +49 (0)351 449210505
E-Mail: Pressestelle@uniklinikum-dresden.de www.uniklinikum-dresden.de
Simon Schmitt
Kommunikation und Medien | Leitung und Pressesprecher
Helmholtz-Zentrum Dresden-Rossendorf
E-Mail: s.schmitt@hzdr.de
Tel.: +49 351 260-3400
www.hzdr.de
Nationales Centrum für Tumorerkrankungen Dresden (NCT/UCC)
Das Nationale Centrum für Tumorerkrankungen Dresden (NCT/UCC) ist eine gemeinsame Einrichtung des Deutschen Krebsforschungszentrums (DKFZ), des Universitätsklinikums Carl Gustav Carus Dresden, der Medizinischen Fakultät der Technischen Universität Dresden und des Helmholtz-Zentrums Dresden-Rossendorf (HZDR).
Das NCT hat es sich zur Aufgabe gemacht, Forschung und Krankenversorgung so eng wie möglich zu verknüpfen. Damit können Krebspatienten an den NCT-Standorten auf dem jeweils neuesten Stand der wissenschaftlichen Erkenntnisse behandelt werden. Gleichzeitig erhalten die Wissenschaftler durch die Nähe von Labor und Klinik wichtige Impulse für ihre praxisnahe Forschung. Gemeinsamer Anspruch der NCT-Standorte ist es, das NCT zu einem internationalen Spitzenzentrum der patientennahen Krebsforschung zu entwickeln. Das Dresdner Zentrum baut auf den Strukturen des Universitäts KrebsCentrums Dresden (UCC) auf, das 2003 als eines der ersten Comprehensive Cancer Center (CCC) in Deutschland gegründet wurde. Seit 2007 wurde das Dresdner Zentrum von der Deutschen Krebshilfe e.V. (DKH) kontinuierlich als „Onkologisches Spitzenzentrum“ ausgezeichnet.
Deutsches Krebsforschungszentrum (DKFZ)
Das DKFZ ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Über 1.300 Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können.
Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, interessierte Bürger und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs.
Gemeinsam mit Partnern aus den Universitätskliniken betreibt das DKFZ das Nationale Centrum für Tumorerkrankungen (NCT) an den Standorten Heidelberg und Dresden, in Heidelberg außerdem das Hopp-Kindertumorzentrum KiTZ. Im Deutschen Konsortium für Translationale Krebsforschung (DKTK), einem der sechs Deutschen Zentren für Gesundheitsforschung, unterhält das DKFZ Translationszentren an sieben universitären Partnerstandorten. Die Verbindung von exzellenter Hochschulmedizin mit der hochkarätigen Forschung eines Helmholtz-Zentrums an den NCT- und den DKTK-Standorten ist ein wichtiger Beitrag, um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Krebspatienten zu verbessern.
Das DKFZ wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.
Universitätsklinikum Carl Gustav Carus Dresden
Das Universitätsklinikum Carl Gustav Carus Dresden bietet medizinische Betreuung auf höchstem Versorgungsniveau. Als Krankenhaus der Maximalversorgung deckt es das gesamte Spektrum der modernen Medizin ab. Das Universitätsklinikum vereint 26 Kliniken und Polikliniken, sechs Institute und 17 interdisziplinäre Zentren, die eng mit den klinischen und theoretischen Instituten der Medizinischen Fakultät zusammenarbeiten.
Mit 1.410 Betten und 201 Plätzen für die tagesklinische Behandlung von Patienten ist das Dresdner Uniklinikum das größte Krankenhaus der Stadt und zugleich das einzige Krankenhaus der Maximalversorgung in Ostsachsen. Rund 1.120 Ärzte decken das gesamte Spektrum der modernen Medizin ab. 2.250 Schwestern und Pfleger kümmern sich um das Wohl der Patienten. Wichtige Behandlungsschwerpunkte des Uniklinikums sind die Versorgung von Patienten, die an Krebs, an Stoffwechsel- und an neurodegenerativen Erkrankungen.
Deutschlands größter Krankenhausvergleich des Nachrichtenmagazins „Focus“ bescheinigt dem Universitätsklinikum Carl Gustav Dresden eine hervorragende Behandlungsqualität. Die Dresdner Hochschulmedizin belegt deshalb Platz fünf im deutschlandweiten Ranking.
Medizinische Fakultät Carl Gustav Carus der Technischen Universität Dresden
Die Hochschulmedizin Dresden, bestehend aus der Medizinischen Fakultät Carl Gustav Carus und dem gleichnamigen Universitätsklinikum, hat sich in der Forschung auf die Bereiche Onkologie, metabolische sowie neurologische und psychiatrische Erkrankungen spezialisiert. Bei diesen Schwerpunkten sind übergreifend die Themenkomplexe Degeneration und Regeneration, Imaging und Technologieentwicklung, Immunologie und Inflammation sowie Prävention und Versorgungsforschung von besonderem Interesse. Internationaler Austausch ist Voraussetzung für Spitzenforschung – die Hochschulmedizin Dresden lebt diesen Gedanken mit Mitarbeiterinnen und Mitarbeitern aus 73 Nationen sowie zahlreichen Kooperationen mit Forschern und Teams in aller Welt.
Helmholtz-Zentrum Dresden-Rossendorf (HZDR)
Das Helmholtz-Zentrum Dresden-Rossendorf (HZDR) forscht auf den Gebieten Energie, Gesundheit und Materie. Folgende Fragestellungen stehen hierbei im Fokus:
• Wie nutzt man Energie und Ressourcen effizient, sicher und nachhaltig?
• Wie können Krebserkrankungen besser visualisiert, charakterisiert und wirksam behandelt werden?
• Wie verhalten sich Materie und Materialien unter dem Einfluss hoher Felder und in kleinsten Dimensionen?
Zur Beantwortung dieser wissenschaftlichen Fragen betreibt das HZDR große Infrastrukturen, die auch von externen Messgästen genutzt werden: Ionenstrahlzentrum, Hochfeld-Magnetlabor Dresden und ELBE-Zentrum für Hochleistungs-Strahlenquellen.
Das HZDR ist Mitglied der Helmholtz-Gemeinschaft, hat fünf Standorte (Dresden, Freiberg, Grenoble, Leipzig, Schenefeld bei Hamburg) und beschäftigt knapp 1.200 Mitarbeiter – davon etwa 500 Wissenschaftler inklusive 170 Doktoranden.